
Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
Orsaker och patogenes för prostataadenom
Medicinsk expert av artikeln
Senast recenserade: 04.07.2025
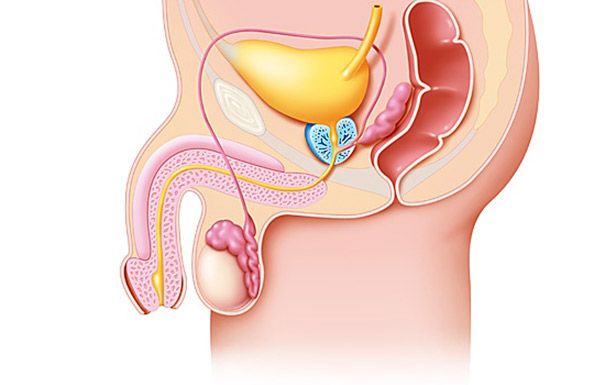
Att förstå patogenesen för prostataadenom (prostatakörteln) är omöjligt utan att ta hänsyn till moderna data om dess anatomi och morfologi. Den moderna teorin om prostataadenomens (prostatakörtelns) utveckling är baserad på det zonala konceptet för prostatastrukturen, enligt vilket flera områden särskiljs i prostatakörteln, vilka skiljer sig åt i de histologiska och funktionella egenskaperna hos de cellulära element som ingår i dem. Dessa är de perifera, centrala och övergångszonerna (transienta), såväl som området för det främre fibromuskulära stromat och det preprostatiska segmentet.
I området kring sädesledaren öppnas utloppsöppningarna från sädesledaren. Väggen i den proximala delen av urinröret består av longitudinella glatta muskelfibrer. Den preprostatiska (genitala) sfinktern, som bildas av ett tjockt lager glatta muskelfibrer, omger den proximala delen av urinröret från urinblåsans hals till toppen av sädesledaren och förhindrar retrograd ejakulation.
Histologiska studier har visat att tillväxten av prostataadenom (prostatakörteln) börjar i prostatans centrala och övergångszoner. Prostatans övergångszon består av två separata körtlar belägna omedelbart bakom urinblåsans inre sfinkter. Utsöndringskanalerna i denna zon är belägna på urinrörets laterala vägg nära sädesvampen. Den proximala övergångszonen innehåller körtlarna i den periuretrala zonen, de gränsar till urinblåsans inre sfinkter och är belägna parallellt med urinrörets axel. Adenomatösa noder kan utvecklas både i övergångszonen och i den parauretrala zonen. Förutom nodulär hyperplasi tenderar övergångszonen att växa med åldern.
Prostatakapseln spelar en viktig roll i utvecklingen av symtom på prostataadenom (prostatakörteln). Hos hundar är prostatakapseln därför dåligt utvecklad, och även vid uttalad hyperplasi uppstår sällan symtom på sjukdomen. Kapseln överför trycket från den förstorade prostatavävnaden till urinröret, vilket orsakar en ökning av urinrörets motstånd.
Prostataadenom (prostatakörteln): patofysiologi
Den prostatiska delen av urinröret är förlängd och deformerad till 4-6 cm eller mer, främst på grund av området av den bakre väggen som är beläget ovanför sädesvampen. Blåsans hals är upphöjd och deformerad, dess lumen blir slitsliknande. Som ett resultat ökar urinrörets naturliga krökning, och med ojämn utveckling av laterala lober blir urinröret också krökt i tvärriktningen, vilket kan resultera i att den kan anta ett sicksackformat utseende. Gap i blåsans halslumen till följd av att uretral-sfinktermekanismen misslyckas under detrusorkompensation manifesteras kliniskt av urininkontinens.
Urinblåsan genomgår också djupgående förändringar. Dess reaktion på utvecklingen av obstruktion går igenom tre steg: irritabilitet, kompensation och dekompensation. I det första stadiet av infravesikal obstruktion reagerar urinblåsan genom att öka detrusorkontraktionerna, vilket möjliggör tillfälligt upprätthållande av funktionell balans och fullständig urintömning. Vidare utveckling av obstruktion leder till kompensatorisk hypertrofi av urinblåsväggen, som kan nå 2-3 cm i tjocklek. I detta fall kan den få ett trabekulärt utseende på grund av förtjockade och utbuktande muskelbuntar.
Det inledande stadiet av trabekelns utveckling kännetecknas morfologiskt av hypertrofi av glatta muskelceller. Processens fortskridande leder till separation av hypertrofierade muskelelement och fyllning av mellanrummen mellan dem med bindväv. Fördjupningar som kallas falska divertiklar bildas mellan trabeklerna, vars väggar gradvis blir tunnare på grund av ökat intravesikalt tryck. Sådana divertiklar är ofta multipla och når ibland betydande storlekar.
Detrusorns elastiska egenskaper bestäms av närvaron av kollagen, vilket i dess glatta muskelvävnad utgör 52 % av den totala mängden protein. När kompensationsförmågan uttöms och atrofin ökar blir blåsans väggar tunnare. Detrusorn förlorar sin förmåga att dra ihop sig och sträcks ut, vilket leder till att blåsans kapacitet ökar avsevärt och når 1 liter eller mer. Samtidiga inflammatoriska och trofiska förändringar leder till uttalad skleros i blåsväggens muskelskikt och en minskning av kollagenhalten. Halten av bindväv blir lika med eller överstiger innehållet av muskelelement.
Graden av återställande av blåsväggens normala struktur beror på hur länge obstruktionen av urinflödet har varit. Som ett resultat av långvarig obstruktion utvecklas irreversibla morfologiska förändringar, vilket leder till uttalade funktionella störningar i urinblåsan och inte kan elimineras ens med kirurgisk behandling. Allvarlig infravesikal obstruktion leder till ökat tryck i urinblåsan, nedsatt urinflöde från njurarna och utveckling av vesikoureteral och renal reflux, samt pyelonefrit. Uretrarna expanderar, förlängs, blir slingrande, ureterohydronefros och kronisk njursvikt utvecklas. Patogenesen för förändringar i njurar och övre urinvägar hos patienter med prostataadenom är komplex och beror på många faktorer: åldersrelaterade förändringar, samtidiga sjukdomar som påverkar deras funktionella förmåga, utveckling av obstruktiv uropati.
I det första stadiet av obstruktiv uropati förhindrar bevarandet av den forniska apparaten i bäckenen och integriteten hos epitelet i papillernas samlande tubuli uppkomsten av njurbäckenreflux och penetration av infektion i njurparenkymet i en uppåtgående riktning. Med utvecklingen av ureterohydronefros sker strukturell deformation av bäckenvalven, vilket skapar gynnsamma förhållanden för uppkomsten av njurbäcken-tubulär och därefter njurbäcken-venös och njurbäcken-lymfatisk reflux.
Som ett resultat av ökat intrapelviskt tryck och njurbäcken-renal reflux försämras njurarnas hemodynamik avsevärt, följt av utveckling av strukturella förändringar i artärerna inom organen i form av deras utplåning och diffus stenos. Hemodynamiska störningar leder till allvarliga metaboliska förändringar och svår njurvävnadsischemi. Obstruktiv uropati resulterar i en progressiv försämring av alla indikatorer på njurarnas funktionella tillstånd. Ett karakteristiskt drag för denna process är en tidig försämring av njurarnas koncentrationsförmåga, vilket främst manifesteras av en kraftig minskning av reabsorptionen av Na-joner och en ökning av deras utsöndring med urin. Nedsatt njurfunktion i stadium I prostataadenom observeras hos 18% av patienterna. I stadium II komplicerar kronisk njursvikt sjukdomsförloppet hos 74%, varav 11% har ett terminalt stadium. Kronisk njursvikt upptäcks hos alla patienter med prostataadenom i stadium III, med intermittent stadium observerat hos 63% och terminalt stadium hos 25% av de undersökta.
Urinvägsinfektion är av fundamental betydelse i patogenesen av njursjukdomar vid prostataadenom och komplicerar sjukdomsförloppet avsevärt. Pyelonefrit och njursvikt står för upp till 40 % av dödsorsakerna hos patienter med prostataadenom. Kronisk pyelonefrit hos patienter med prostataadenom observeras i 50–90 % av fallen.
Inflammation av bakteriellt ursprung förekommer huvudsakligen i den interstitiella peritubulära vävnaden. I patogenesen av sekundär pyelonefrit vid prostataadenom spelas huvudrollen av urostas, utveckling av vesikoureteral och njurbäckenreflux. Infektionen går in i njuren genom att stiga upp från urinblåsan. Urinvägsinfektion åtföljer de flesta fall av prostataadenom. Kronisk cystit observerades hos 57–61 % av öppenvårdspatienter och 85–92 % av inneliggande patienter. I detta avseende kan patogenesen av kronisk pyelonefrit hos patienter med prostataadenom representeras enligt följande: infravesikal obstruktion → blåsdysfunktion → cystit → insufficiens i vesikoureterala övergångar → vesikoureteral reflux → kronisk pyelonefrit.
Förekomsten av samtidig inflammatorisk process i prostatan spelar en stor roll i bildandet av den kliniska bilden vid prostataadenom. Frekvensen av kronisk prostatit vid prostataadenom enligt laboratorie-, kirurgiska och obduktionsdata är 73, 55,5 respektive 70 %. Venös stas, kompression av acini-utsöndringskanalerna av körtelns hyperplastiska vävnad och dess ödem är förutsättningar för utveckling av kronisk inflammation. Morfologisk undersökning av det kirurgiska materialet visade att den inflammatoriska processen i de flesta fall var lokaliserad i körtelns periferi. Samtidig kronisk prostatit kan kliniskt manifestera sig som dysuri, vilket kräver differentialdiagnos med urineringsstörningar orsakade av själva prostataadenomet. Dess närvaro leder också till en ökning av antalet tidiga och sena postoperativa komplikationer, i samband med vilka åtgärder behövs för att identifiera och sanera kronisk prostatit i skedet av konservativ behandling eller förberedelse för kirurgi.
Blåsstenar vid adenom bildas sekundärt på grund av störningar i blåstömningen. De upptäcks hos 11,7–12,8 % av patienterna. De har vanligtvis en regelbunden rund form, kan vara enstaka eller flera, och enligt kemisk sammansättning är de urater eller fosfater. Njurstenar följer med prostataadenom i 3,6–6,0 % av fallen.
En vanlig komplikation av prostataadenom är fullständig akut urinretention, som kan utvecklas i vilket skede som helst av sjukdomen. I vissa fall är detta kulmen på den obstruktiva processen i kombination med dekompensation av detrusorns kontraktila förmåga, medan det i andra fall utvecklas plötsligt mot bakgrund av måttliga symtom på urineringsstörningar. Ofta är detta den första kliniska manifestationen av prostataadenom. Enligt litteraturen observeras denna komplikation hos 10-50% av patienterna, oftast förekommer den i stadium II av sjukdomen. Provocerande faktorer för utvecklingen av denna komplikation kan vara en dietstörning (intag av alkohol, kryddor), hypotermi, förstoppning, för tidig tömning av blåsan, stress, intag av vissa läkemedel (antikolinerga läkemedel, lugnande medel, antidepressiva medel, diuretika).
De viktigaste faktorerna för utvecklingen av akut urinretention är tillväxten av hyperplastisk vävnad, funktionella förändringar i nack- och blåsans muskeltonus och nedsatt mikrocirkulation i bäckenorganen med utveckling av prostataödem.
I det initiala skedet av akut urinretention leder ökad kontraktil aktivitet hos detrusorn till en ökning av det intravesikala trycket. I efterföljande skeden, på grund av sträckning av blåsväggen och en minskning av dess kontraktila förmåga, sjunker det intravesikala trycket.

